本网讯(通讯员钦闪闪)近日,我校太阳集团官网8722钦闪闪教授团队在Science Advances发表题为Transcobalamin 1 is a keratinocyte-derived autoantigen driving psoriasis through T helper 17 cell activation的研究论文。

银屑病(Psoriasis)是一种典型的由遗传易感性与环境因素相互作用驱动的慢性系统性自身免疫性疾病,全球患者超过1.25亿人。若将遗传背景视为发病的“土壤”,环境诱因则是点燃疾病的“火花”。在易感个体中,心理应激、链球菌感染、特定药物、吸烟、酗酒、肥胖及尼古丁依赖等多种环境因素均可触发或加重银屑病病情。然而,这些外部环境信号究竟如何突破免疫耐受,启动针对自身的免疫攻击,其深层分子机制长期以来一直如同一个未被打开的“黑箱”。
表观遗传修饰因其对环境信号的高度敏感性,被认为是连接外部刺激与基因组响应的关键桥梁。与此同时,自身抗原(Autoantigens)在自身免疫病的发病机制中扮演着核心角色。在正常情况下,免疫系统对“自身”成分具有耐受性。但在病理条件下,某些自身组织成分被免疫系统误认为“异己”,从而引发级联免疫反应。基于此,该研究团队提出了一种创新性假说:环境因素与遗传易感性的相互作用,可能导致表观遗传修饰(如DNA甲基化)发生异常,从而“唤醒”了原本沉默的自身抗原,进而触发自身免疫应答。
为验证上述假说,钦闪闪教授团队另辟蹊径,创新性地整合了DNA甲基化组、转录组和免疫肽组三类多维数据,建立了一套高通量筛选策略,专门用于捕捉因DNA低甲基化而异常激活的银屑病相关自身抗原。通过该策略,研究团队最终精准锁定转钴胺素1(Transcobalamin 1, TCN1)为银屑病关键致病自身抗原。
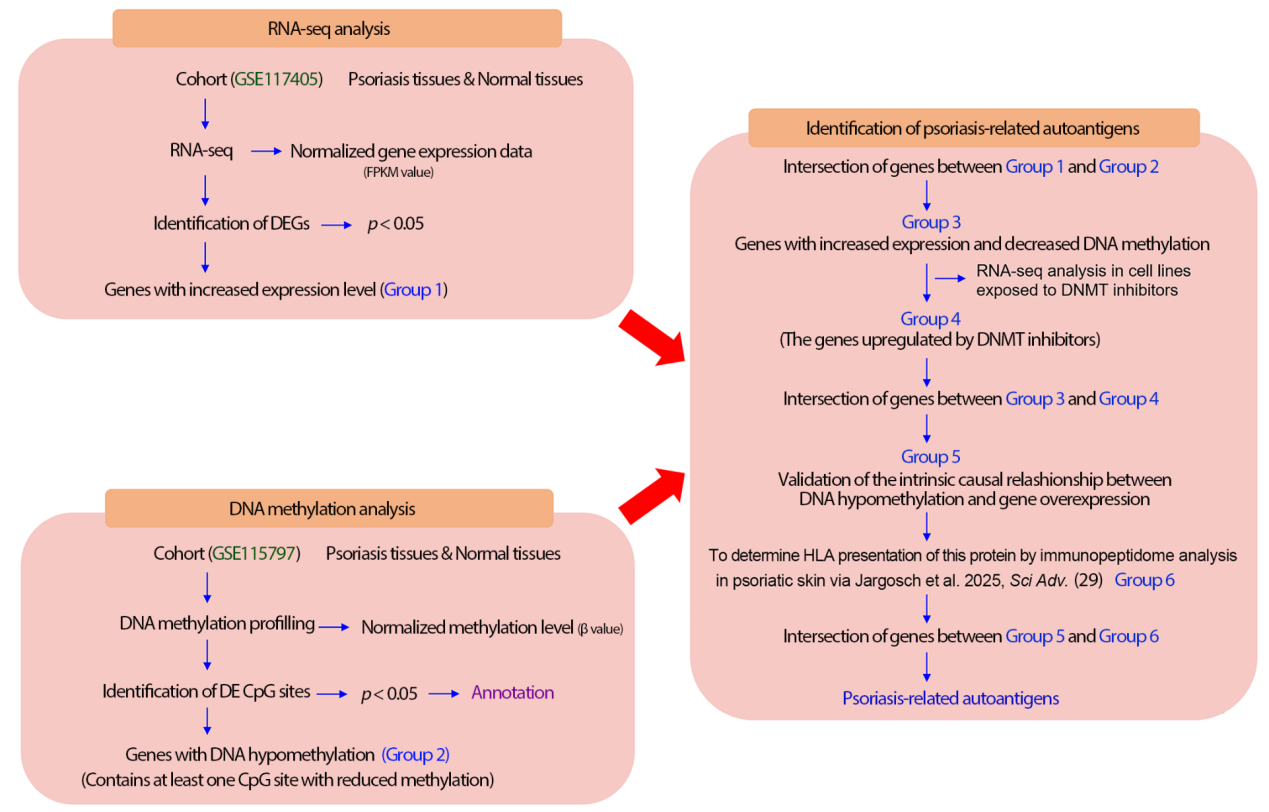
本研究主要有以下亮眼科学发现:
多组学分析鉴定到10个受DNA低甲基化而异常激活的银屑病自身抗原,其中SERPINB3、SERPINB4、RSAD2、NCCRP1、PI3能同时被HLA-I/II识别呈递;EPHX3、KRT16、ARL11、IFI6特异被HLA-I识别呈递;TCN1特异被HLA-II识别呈递。
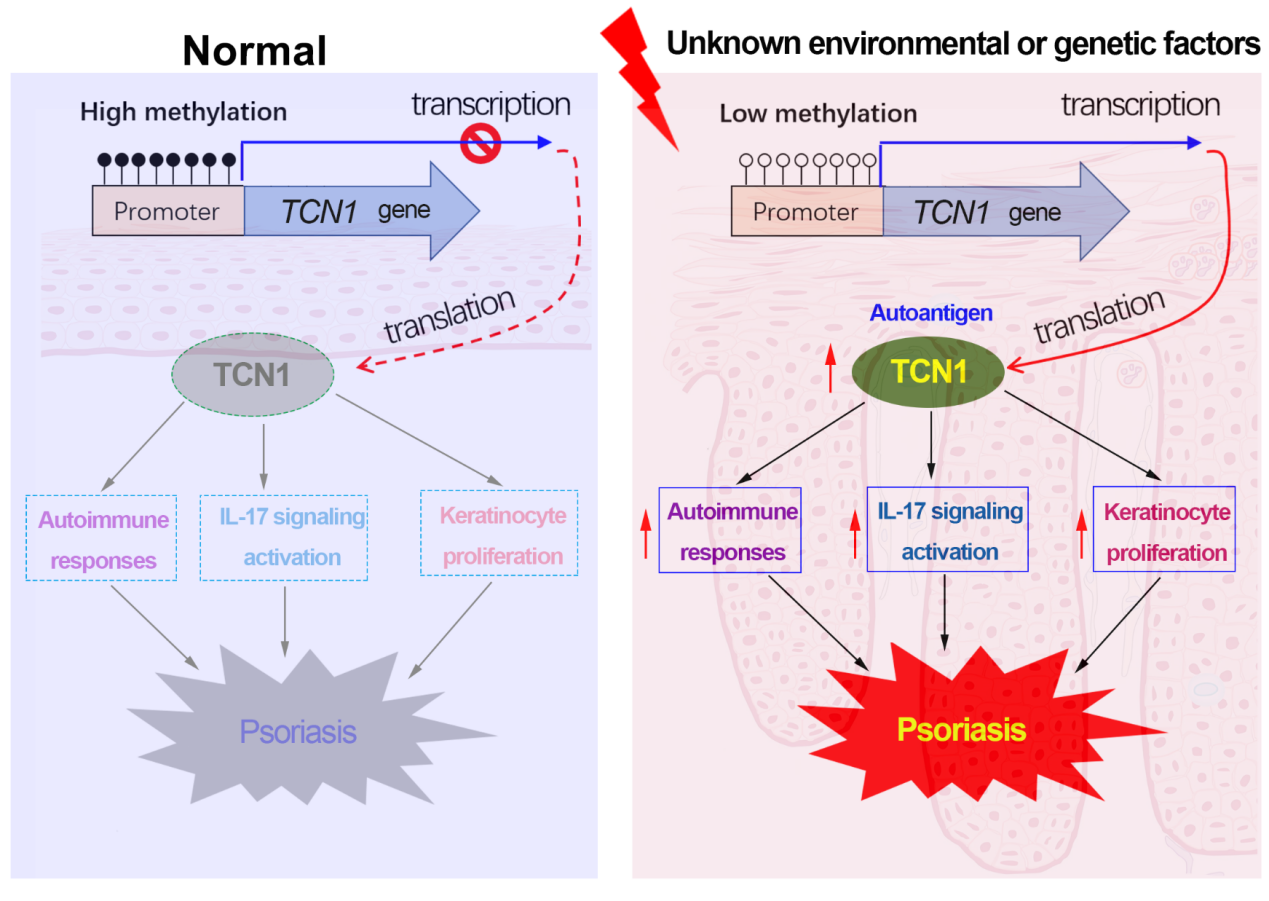
在正常皮肤中TCN1基因几乎不表达,但在银屑病皮损中因启动子区DNA低甲基化而被异常"唤醒",表达量显著升高。
通过单细胞测序和多重免疫组织化学技术,研究证实TCN1特异性表达于银屑病皮损中的角质形成细胞(包括棘层、颗粒层和增殖期角质形成细胞)。
TCN1是一个分泌蛋白,来源于角质形成细胞。银屑病患者血清TCN1水平显著高于健康对照,提示其可作为银屑病血清生物标志物。
TCN1表达与角质形成细胞增殖显著正相关。角质形成细胞内TCN1上调能直接促进细胞增殖,并且这种促增殖作用不依赖于其分泌形式。
作为自身抗原,由角质形成细胞分泌到胞外的TCN1蛋白可被树突状细胞摄取,经HLA-II类分子提呈给CD4⁺ T细胞,促进其向致病性Th17细胞分化,产生IL-17A等关键炎症因子,形成"炎症-增殖"恶性循环。
由于TCN1基因在常用模式动物(如小鼠、大鼠)中缺失,提示传统小鼠银屑病模型无法真实反映人类银屑病病程。研究还提示未来需要开发非人灵长类、犬或猪等TCN1表达物种的银屑病模型,以更准确地模拟人类疾病机制。
综上,本研究不仅证实了"环境刺激—表观修饰改变—自身抗原激活—银屑病"这一致病假说,系统鉴定了10个由DNA低甲基化异常激活的银屑病相关自身抗原,更是首次揭示了一个同时驱动角质形成细胞过度增殖和Th17免疫应答的"枢纽分子"——TCN1。一方面,胞内TCN1直接促进角质形成细胞增殖;另一方面,分泌型TCN1作为自身抗原被抗原提呈细胞摄取并经HLA-II类分子提呈,激活CD4⁺ T细胞向Th17方向分化,进而放大IL-17炎症信号。这一发现不仅深化了对银屑病表观遗传-免疫-增殖三联病理机制的认识,更为开发针对TCN1的靶向干预策略(如表观遗传调控、中和抗体或阻断分泌等)提供了全新的理论基础和临床转化方向。
太阳网集团tyc8722钦闪闪教授为本文通讯作者;太阳网集团tyc8722附属江夏区第一人民医院王晶博士、太阳集团官网8722李丹丹教授为共同第一作者。首都医科大学北京朝阳医院何焱玲教授为本研究提供了重要专业支持。本研究得到国家自然科学基金、湖北省医学青年拔尖人才项目、湖北省自然科学基金联合基金、太阳网集团tyc8722生物医药研究院PI项目、太阳集团官网8722高峰计划等经费资助。
原文链接:https://www.science.org/doi/10.1126/sciadv.adv6716.(审稿 杜伯雨)
